Lanthane, La, numéro atomique 57
général
Lanthane [lantaːn] est un élément chimique avec le symbole d'élément La et le numéro atomique 57. Il fait partie des métaux de transition ainsi que des métaux des terres rares. Dans le tableau périodique, il se trouve dans le 6. Période et le 3. Sous-groupe (groupe 3) ou groupe du scandium. Généralement, il est également compté dans le Lanthanoiden, même si la f-shell de l'élément est inoccupée.
Lanthane (grec λανθάνειν, lanthanein, "être caché") 1839 a été découvert par le chimiste et chirurgien suédois Carl Gustav Mosander. D'un nitrate de cérium supposé pur, il a obtenu par cristallisation fractionnée le sulfate de Lanthane.
Le lanthane ne se trouve naturellement que dans les composés chimiques associés à d'autres lanthanides dans divers minéraux. Ce sont principalement:
Monazite ((Ce, La, Th, Nd, Y) PO4)
Bastnäsit ((Ce, La, Y) CO3F)
Récupération
Après une séparation complexe de l'autre compagnon de lanthanide, l'oxyde est mis à réagir avec du fluorure d'hydrogène en fluorure de lanthane. Ensuite, il est réduit en lanthane avec du calcium pour former du fluorure de calcium. La séparation des résidus de calcium et des impuretés restants a lieu dans une refusion supplémentaire sous vide.
Traits
Le métal blanc argenté est malléable et ductile. Il y a trois modifications métalliques.
Lanthane est indigne. Il se recouvre rapidement d'une couche d'oxyde blanc dans l'air, qui réagit dans l'air humide sur l'hydroxyde.
À des températures supérieures à 440 ° C, le lanthane brûle en oxyde de lanthane (La2O3). La formation d'hydrogène dans l'eau froide est lente, dans l'eau chaude une réaction rapide à l'hydroxyde. Dans les acides dilués, le lanthane se dissout sous l'action de l'hydrogène et réagit directement à la chaleur avec les halogènes, même à température ambiante. Le lanthane et l'hydrogène forment un hydrure non stœchiométrique noir sensible à l'eau.
Utiliser
Le lanthane est un composant du misch metal. Les matériaux de silex pyrophoriques contiennent 25 à 45 pour cent en poids de lanthane. En outre, il est utilisé comme agent réducteur en métallurgie. En tant qu'addition de fonte, il favorise la formation de graphite sphéroïdal, en tant qu'additif d'alliage, il améliore la résistance à l'oxydation. Les adjuvants de lanthane réduisent la dureté et la sensibilité à la température du molybdène.
Les cathodes de haute qualité permettant de générer des électrons libres sont constituées d’hexaborure de lanthane en remplacement du fil de tungstène. L’oxyde de lanthane de haute pureté est utilisé dans l’industrie du verre pour la production de verres de haute qualité à indice de réfraction élevé pour l’optique z. B. utilisé pour les objectifs de la caméra.
Avec du cobalt:
Le LaCo5 en alliage cobalt-lanthane est utilisé comme matériau magnétique, le titanate de baryum dopé au lanthane, pour la fabrication de thermistances CTP (résistances dépendant de la température). En conjonction avec le cobalt, le fer, le manganèse, le strontium et autres, il sert de cathode pour les piles à combustible à haute température (SOFC). Le nickel de lanthane "contaminé" (LaNi5) est utilisé comme stockage d'hydrogène dans les batteries d'accumulateurs au nickel-métal hydrure. En outre, il existe dans les lampes à arc au carbone pour l'éclairage de studio et dans les systèmes de projection de film (application historique?) Avant.
Avec du titane:
Alliage de métaux avec des compositions de lanthane et de titane, cet effet est attribué au fait qu’avec le traitement de formation de copeaux, la longueur des copeaux est réduite. Cela devrait faciliter le traitement du métal.
Dans le domaine de la médecine, des instruments résistant à la corrosion et facilement stérilisables sont fabriqués à partir du métal d'alliage. On dit que cet alliage métallique à base de titane convient particulièrement bien aux outils et appareils chirurgicaux, car la propension à l’allergie de l’utilisation de cet alliage métallique avec le titane par rapport à d’autres alliages devrait être faible.
En tant qu'oxyde de lanthane
Production de verres (Lanthanglas) à indice de réfraction relativement élevé, qui ne varie que très peu avec la longueur d'onde (faible dispersion), pour les appareils photo, les lentilles de télescope et les verres de lunettes
Production de vitraux en cristal et de porcelaine. Il remplace des composés de plomb plus toxiques par une amélioration simultanée de la résistance chimique (amélioration de la résistance aux alcalis, "lave-vaisselle")
Addition de catalyseur aux zéolithes lors du craquage catalytique fluide dans la raffinerie
Production de masses de condensateur en céramique et de verres sans silicate
Composant des polisseurs de verre
Production de cathodes chaudes pour tubes électroniques (également borures de lanthane)
En tant que carbonate de lanthane
Médicament destiné à réduire le taux de phosphate chez les patients dialysés (appelé «liant de phosphate»)
Le lanthane est classé comme toxicité faible. Une dose toxique est inconnue. Cependant, la poudre de lanthane est considérée comme hautement corrosive car elle réagit très facilement, par exemple en cas d'humidité de la peau, à l'hydroxyde de lanthane basique (similaire aux éléments calcium et strontium). La dose létale chez le rat est de 720 mg.
| Général | |
| Nom, symboleOrdre numéro | Lanthane, La, 57 |
| La Gamme | Les métaux de transition |
| Groupe, période, bloc | 3, 6, d |
| Apparence | blanc argenté |
| numéro CAS | 7439-91-0 |
| Fraction de masse de l'enveloppe terrestre | 17 ppm |
| nucléaire | |
| masse atomique | 138,9055 u |
| rayon atomique | 195 pm |
| Rayon covalent | 207 pm |
| Elektronenkonf. | [Xe] 5d (1) 6s2 |
| 1. ionisation | 538,1 KJ / mol |
| 2. ionisation | 1067 KJ / mol |
| 3. ionisation | 1850 KJ / mol |
| physiquement | |
| L'état physique | fest |
| la structure cristalline | hexagonal |
| densité | 6,17 g / cm3 (20 ° C) |
| magnétisme | paramagnétique (m = 5,4 * 10 (-5)) |
| point de fusion | 1193 K (920 C) |
| point d'ébullition | 3743 K (3470 C) |
| Volume molaire | 22,39 * 10 (-6) m (3) / mol |
| Chaleur de vaporisation | 400 KJ / mol |
| la chaleur de fusion | 6,2 KJ / mol |
| Conductivité électrique | 1,626 * 10 (6) A / (V * m) |
| conductivité thermique | 13 W / (m * K) |
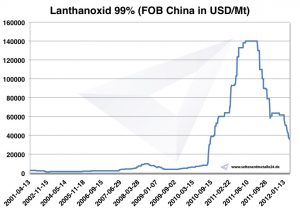
Prix du lanthane