Hafnium est un élément chimique avec le symbole Hf et le numéro atomique 72. Il est nommé d'après le nom latin de la ville de Copenhague, Hafniadans lequel l'élément a été découvert. Il s'agit d'un métal de transition gris argenté brillant et résistant à la corrosion qui appartient au 4ème sous-groupe (groupe 4) ou au groupe titane du tableau périodique.
Le hafnium a des propriétés très similaires à celles du zirconium directement au-dessus dans le tableau périodique. Les fonctions biologiques ne sont pas connues, elles ne se produisent normalement pas dans l'organisme humain et elles ne sont pas toxiques.
Hafnium a été l'un des derniers éléments stables du tableau périodique à être découvert. La première indication de l'existence d'un autre élément entre le lutétium et le tantale est née de la loi de Moseley trouvée en 1912. En 1914, Henry Moseley a tenté de trouver l'élément inconnu mais attendu avec le numéro atomique 72 selon cette loi dans des échantillons de minéraux de terres rares (aujourd'hui lanthanides). Mais il n'a pas réussi.
Dans son ouvrage sur la théorie atomique publié en 1922, Niels Bohr prédit que la série des lanthanides avec lutétium prendrait fin et que l'élément 72 doit donc être similaire au zirconium. Le hafnium pourrait être détecté juste un an plus tard: en 1923, Dirk Coster et George de Hevesy l'ont découvert à Copenhague en utilisant la spectroscopie aux rayons X dans le zirconium norvégien. Des recherches plus poussées sur d'autres minéraux ont montré que le hafnium est toujours contenu dans des minéraux contenant du zirconium. Jantzen et Hevesy ont réussi à les séparer du zirconium en cristallisant à plusieurs reprises les fluorures de diammonium et de dipotassium des deux éléments. L'hafnium élémentaire pourrait alors être obtenu par réduction avec du sodium.
Occurrence
L'hafnium, avec une teneur de 4,9 ppm dans la croûte continentale, est un élément peu courant sur terre. En termes de fréquence, il est comparable aux éléments brome et césium et plus commun que l'or et le mercure connus depuis longtemps. Hafnium ne se produit pas naturellement ou dans ses propres minéraux. Les minéraux de zirconium tels que le zircon et la baddeleyite, en revanche, contiennent toujours du hafnium; la quantité d'hafnium est généralement de 2% de la teneur en zirconium (1 à 5% en poids d'hafnium). L'un des rares minéraux qui contiennent plus d'hafnium que le zirconium est la variété de zircon Alvit [(Hf, Th, Zr) SiO4].
Comme pour le zirconium, les gisements d'hafnium les plus importants sont les gisements de zirconium en Australie et en Afrique du Sud. Les réserves sont estimées à 1,1 million de tonnes (calculées en oxyde d'hafnium).
Extraction et présentation
Afin d'obtenir de l'hafnium, il doit être séparé du zirconium. Cela n'est pas possible pendant le processus de fabrication, mais a lieu dans un processus séparé. Des procédés d'extraction sont utilisés pour la séparation. La solubilité différente de certains sels de zirconium et d'hafnium dans des solvants spéciaux est utilisée. Des exemples en sont les différentes solubilités des nitrates dans le phosphate de tri-n-butyle et celle des thiocyanates dans la méthylisobutylcétone. D'autres options de séparation possibles sont les échangeurs d'ions et la distillation fractionnée de composés appropriés.
Après le procédé Kroll, l'hafnium séparé peut d'abord être converti en chlorure d'hafnium (IV) puis réduit en hafnium élémentaire avec du sodium ou du magnésium.
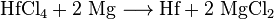
Si un hafnium encore plus pur est requis, le procédé Van Arkel de Boer peut être utilisé. Lors du chauffage sous vide, l'hafnium réagit initialement avec l'iode pour former de l'iodure d'hafnium (IV). Celui-ci est à nouveau décomposé en hafnium et en iode sur un fil chaud.

Le hafnium n'est produit qu'en petites quantités à une échelle de 100 tonnes. Il n'est pas produit en interne, mais est un sous-produit de l'extraction de zirconium sans hafnium pour les barres de combustible.
Propriétés
Propriétés physiques

Structure cristalline de α-Hf, a = 320 pm,c = 505 pm
L'hafnium est un métal lourd argenté et brillant de haute densité (13,31 g / cm3). Il cristallise en deux modifications différentes en fonction de la température. Dans des conditions normales, il cristallise dans un empilement fermé hexagonal de sphères (α-Hf) et est donc isotypique à α-Zr, au-dessus de 1775 ° C, il se transforme en une structure cubique centrée sur le corps (β-Hf).
Si la pureté du hafnium est élevée, il est relativement doux et souple. Il est facile de travailler par roulage, forgeage et martelage. Si, au contraire, il y a des traces d'oxygène, d'azote ou de carbone dans le matériau, il devient cassant et difficile à traiter. Les points de fusion et d'ébullition de l'hafnium sont les plus élevés du groupe à 2227 ° C et 4450 ° C (point de fusion: titane: 1667 ° C, zirconium: 1857 ° C).
Dans presque toutes les autres propriétés, le métal ressemble à son homologue plus léger, le zirconium. Ceci est causé par la contraction du lanthanide, qui se traduit par des rayons atomiques et ioniques similaires (rayons atomiques Zr: 159 pm, Hf: 156 pm). Une exception est la densité du zirconium avec 6,5 g / cm3 a une valeur nettement inférieure. Une différence techniquement importante est que l'hafnium peut absorber les neutrons 600 fois mieux. C'est la raison pour laquelle le hafnium doit être séparé pour l'utilisation du zirconium dans les centrales nucléaires.
L'hafnium est supraconducteur en dessous de la température de transition de 0,08 K.
Propriétés chimiques
L'hafnium est un métal de base qui réagit avec l'oxygène pour former du dioxyde d'hafnium lorsqu'il est chauffé. D'autres non-métaux, tels que l'azote, le carbone, le bore et le silicium, forment également des composés dans ces conditions. Une couche d'oxyde dense se forme rapidement à température ambiante, ce qui passive le métal et le protège d'une oxydation supplémentaire.
L'hafnium est stable dans la plupart des acides en raison de sa passivation dans des conditions normales. Il se corrode rapidement dans l'acide fluorhydrique; une corrosion notable se produit dans l'acide sulfurique et phosphorique concentré chaud. Les mélanges d'acide chlorhydrique et d'acide nitrique, y compris l'eau régale, ne doivent être exposés au hafnium que pendant une courte période, même à température ambiante; à 35 ° C, des taux d'élimination supérieurs à 3 mm / an doivent être attendus. Dans les bases aqueuses, il résiste jusqu'à une température d'environ 100 ° C, l'enlèvement de matière est généralement inférieur à 0,1 mm / an.
isotope
Il existe au total 35 isotopes et 18 isomères nucléaires de l'hafnium 153Hf à 188Hf connu. L'hafnium naturel est un élément mixte composé d'un total de six isotopes différents. L'isotope le plus courant est avec une fréquence de 35,08% 180Hf. Il suit 178Hf avec 27,28%, 177Hf avec 18,61%, 179Hf avec 13,62%, 176Hf avec 5,27% et 174Hf à 0,16%. Le seul isotope naturel est 174Hf faiblement radioactif, c'est un émetteur alpha avec une demi-vie de 2 x 1015 Années. Les isotopes 177Hf et 179Hf peut être détecté à l'aide de la spectroscopie RMN.
L'isomère central 178 2mAvec une demi-vie de 31 ans, Hf a une longue durée de vie et émet en même temps un fort rayonnement gamma de 2,45 MeV lorsqu'il se désintègre. Il s'agit de l'énergie la plus élevée émise par un isotope stable sur une longue période. Une application possible consiste à utiliser cet isomère central comme source dans des lasers puissants. En 1999, Carl Collins a découvert que l'isomère pouvait libérer son énergie d'un seul coup lorsqu'il était exposé aux rayons X. Cependant, des applications possibles, telles que les explosifs, sont peu probables.
Utiliser
Feuille de hafnium à partir de déchets industriels
Parce qu'il est difficile à extraire, l'hafnium n'est utilisé qu'en petites quantités. Le principal domaine d'application est la technologie nucléaire, dans laquelle l'hafnium est utilisé comme barre de commande pour réguler la réaction en chaîne dans les réacteurs nucléaires. L'utilisation de l'hafnium présente plusieurs avantages par rapport à d'autres éventuelles substances absorbant les neutrons. L'élément est très résistant à la corrosion et la réaction nucléaire avec les neutrons crée des isotopes d'hafnium, qui ont également des sections efficaces d'absorption. En raison de son prix élevé, il ne convient souvent qu'aux applications militaires, par exemple pour les réacteurs des sous-marins nucléaires.
Il existe quelques autres utilisations. L'hafnium réagit rapidement avec de petites quantités d'oxygène et d'azote et peut donc être utilisé comme substance getter pour éliminer les plus petites quantités de ces substances des systèmes à ultra-vide. Lorsqu'il est brûlé, le métal émet une lumière très vive. Il est donc possible d'utiliser du hafnium dans des lampes flash avec un rendement lumineux particulièrement élevé. Plusieurs composés très stables et à point de fusion élevé, en particulier le nitrure d'hafnium et le carbure d'hafnium, peuvent être fabriqués à partir des éléments.
Dans les alliages avec des métaux tels que le niobium, le tantale, le molybdène et le tungstène, une addition de 2% d'hafnium augmente la résistance. Des matériaux particulièrement stables, à point de fusion élevé et résistants à la chaleur sont créés.
Sicherheitshinweise
Comme beaucoup d'autres métaux, l'hafnium est hautement inflammable et pyrophorique dans son état finement divisé. En revanche, à l'état compact, il n'est pas inflammable. Le métal n'est pas toxique. Pour ces raisons, aucune règle de sécurité particulière ne doit être observée lors de la manipulation de l'hafnium.
Liens
Hafnium forme un certain nombre de composés. Ce sont pour la plupart des sels ou des cristaux mixtes et ont souvent des points de fusion élevés. L'état d'oxydation le plus important de l'hafnium est + IV, mais il existe également des composés dans des états d'oxydation inférieurs, de 0 à + III, et dans des complexes également des états d'oxydation négatifs.
L'oxyde d'hafnium (IV)
L'oxyde d'hafnium (IV) est un solide très stable et à point de fusion élevé. Il a une permittivité relative élevée de 25 (à titre de comparaison: dioxyde de silicium: 3,9). Il peut donc être utilisé comme diélectrique à k élevé pour isoler la connexion de commande (grille) des microprocesseurs. En réduisant encore les largeurs de structure, les courants de fuite deviennent un problème de plus en plus grand, car la miniaturisation des structures CMOS nécessite également une isolation de grille plus fine. Le courant de fuite indésirable augmente fortement en dessous de 2 nm en raison de l'effet tunnel. En utilisant un diélectrique à k élevé, l'épaisseur du diélectrique peut être à nouveau augmentée afin de réduire le courant de fuite sans que le transistor n'ait une perte de performance (réduction de la vitesse de commutation). Ainsi, des diélectriques plus épais permettent une miniaturisation supplémentaire.
Autres composés d'hafnium
Le carbure d'hafnium est l'une des substances ayant les points de fusion les plus élevés. Avec le nitrure d'hafnium et le borure d'hafnium, c'est l'un des matériaux durs.
Il existe des composés halogénés d'hafnium connus. À l'état d'oxydation + IV, il existe à la fois du fluorure et du chlorure, du bromure et de l'iodure. Le chlorure de hafnium (IV) et l'iodure de hafnium (IV) jouent un rôle dans la production de hafnium. Dans les états d'oxydation inférieurs, seuls les composés de chlore et de brome et l'iodure de hafnium (III) sont connus.
L'hexafluoridohafnate de potassium (IV) K2[HfF6], ainsi que l’hexafluoridohafnate d’ammonium (IV) (NH4)2[HfF6] peut être utilisé pour séparer l'hafnium du zirconium, car les deux sels sont plus solubles que les complexes de zirconium correspondants.
| Général | |||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nom, symbole, numéro atomique | Hafnium, Hf, 72 | ||||||||||||||||||||||||||||||||||||||||||||||||
| La Gamme | Les métaux de transition | ||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, période, bloc | 4, 6, j | ||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | gris acier | ||||||||||||||||||||||||||||||||||||||||||||||||
| numéro CAS | 7440-58-6 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Fraction de masse de la coquille de terre | 4,2 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||
| nucléaire | |||||||||||||||||||||||||||||||||||||||||||||||||
| masse atomique | 178,49 unités | ||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique (calculé) | 155 (208) après-midi | ||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon covalent | 150 pm | ||||||||||||||||||||||||||||||||||||||||||||||||
| configuration électronique | [Xe] 4f14 5d2 6s2 | ||||||||||||||||||||||||||||||||||||||||||||||||
| 1. ionisation | 658,5 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 2. ionisation | 1440 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 3. ionisation | 2250 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 4. ionisation | 3216 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| physiquement | |||||||||||||||||||||||||||||||||||||||||||||||||
| L'état physique | fest | ||||||||||||||||||||||||||||||||||||||||||||||||
| modifications | deux (α- / β-Hf) | ||||||||||||||||||||||||||||||||||||||||||||||||
| la structure cristalline | hexagonal | ||||||||||||||||||||||||||||||||||||||||||||||||
| densité | 13,28 g / cm3 (25 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| dureté Mohs | 5,5 | ||||||||||||||||||||||||||||||||||||||||||||||||
| magnétisme | paramagnétique ( = 7,0 10-5) = 7,0 10-5) |
||||||||||||||||||||||||||||||||||||||||||||||||
| point de fusion | 2506 K (2233 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| point d'ébullition | 4876 K (4603 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molaire | 13,44 · 10-6 m3/ mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur de vaporisation | 630 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| la chaleur de fusion | 25,5 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| la pression de vapeur | 0,00013 Pa à 1970 K. | ||||||||||||||||||||||||||||||||||||||||||||||||
| vitesse du son | 3010 m / s à 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||
| Capacité thermique spécifique | 140 J / (kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité électrique | 3,12 · 106 A / (V · m) | ||||||||||||||||||||||||||||||||||||||||||||||||
| conductivité thermique | 23 W / (m K) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Chimique | |||||||||||||||||||||||||||||||||||||||||||||||||
| états d'oxydation | 4 | ||||||||||||||||||||||||||||||||||||||||||||||||
| potentiel normal | −1,505 V (HfO2 + 4 H.+ + 4 e- → Hf + 2 H2O) |
||||||||||||||||||||||||||||||||||||||||||||||||
| électronégativité | 1,3 (échelle de Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||
| isotope | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| propriétés RMN | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||



